*僅供醫學專業人士閱讀參考

一例BRAF V600E突變晚期肺腺癌患者的一線治療經過。
基因突變已成為非小細胞肺癌(NSCLC)已知的致癌因素,而BRAF基因是繼EGFR基因、ALK基因和ROS1基因之後,NSCLC又一個重要的驅動基因,其最常見的突變位點為BRAF V600E。達拉非尼+曲美替尼治療BRAF突變晚期NSCLC的療效非常顯著,並已經獲得了國內外權威指南的一致推薦,作為此類患者的標準治療方案[1-3]。本期“少靶實戰薈”將分享一例達拉非尼+曲美替尼一線治療BRAF V600E突變晚期NSCLC患者的全程診療經過。
該例患者初診為BRAF V600E突變 Ⅳ期NSCLC,合並多發轉移。經達拉非尼+曲美替尼一線長期治療,腫瘤標志物水平迅速下降並且長期維持較低水平,療效長期維持部分緩解(PR),無進展生存期(PFS)達24個月。該病例由廣西醫科大學第一附屬醫院顏雪馨教授提供,並邀請廣西醫科大學第一附屬醫院卜慶教授進行點評。
病例簡介
一、基本情況
基本信息:患者男,63歲,體力狀態(PS)評分0-1分。
初診時間:2021年3月。
主訴:肺癌術後1月餘。
既往史:既往有結核病史,規律抗癆1年;有10年吸煙史,約20支/天。
現病史:2021年2月7日因“左肺占位”在我院胸外科行單孔胸腔鏡下左肺舌段切除術。 術後病理:肺浸潤性腺癌,緊鄰被膜見一腫物,大小2.5x2x1.5cm,免疫組化:TTF-1*(+),CK7(+),NapsinA*(+),Calretinin(-),CK20(-),CK5/6(-),P40(-),P63(散在弱+),Vimentin(-),Ki-67#(熱點區+,10%)。淋巴結:(5組淋巴結)淋巴結1枚,未見癌轉移(0/1),(7組淋巴結)淋巴結2枚,均未見癌轉移(0/2),(9組淋巴結)淋巴結2枚,均未見癌轉移(0/2)。
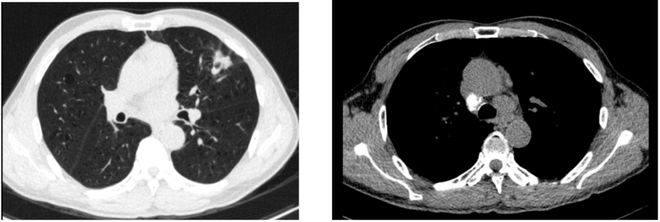
圖1. 術前CT
入院檢查:2021年3月1日,患者入院。顱腦胸腹盆增強CT提示,左肺腺癌術後,縱膈淋巴結轉移,肝多發轉移。骨ECT未見明顯異常。

圖2. 2021年3月1日CT
基因檢測:結果提示存在BRAF V600E突變,高腫瘤突變負荷(TMB-H)。
臨床診斷:左肺腺癌IV期(T1cN2M1c、BRAF V600E陽性、TMB-H、PD-L1未明),合並肺門、縱膈淋巴結轉移,以及肝轉移。
二、治療經過
2021年3月10日,患者開始達拉非尼(150mg bid)+曲美替尼(2mg qd)治療。2021年5月,療效評估為PR。

圖3. 2021年5月CT
2021年5月8日,腫瘤標志物水平顯著下降。患者每2個月定期返院復查,發現腫瘤標志物長期維持在較低水平。

圖4. 腫瘤標志物水平
2021年5月、7月、9月和11月的CT復查結果顯示,病情持續PR。

圖5. 2021年3月-11月CT
在治療期間,2021年6月17日,患者出現畏寒高熱,體溫39.5℃,完善相關感染篩查,未見感染相關指標升高,考慮藥物所致。停藥並予佈洛芬對癥處理,患者第2天體溫恢復正常,第3天繼續達拉非尼+曲美替尼治療,未再出現發熱。2021年7月1日,患者出現第2次畏寒高熱,予佈洛芬處理後仍有反復發熱。患者口服潑尼松(10mg/d)5日,體溫恢復正常,繼續達拉非尼+曲美替尼原劑量治療。2021年10月7日,患者出現第3次發熱,患者口服潑尼松(10mg/d)5日,將達拉非尼的劑量由150mg bid降至100mg bid,曲美替尼維持原劑量治療。減量後的CT復查結果顯示,仍在持續PR,PFS達24個月。

圖6. 2021年11月-2022年4月CT

圖7. 2022年4月-2023年3月CT
專傢點評
卜慶教授:達拉非尼+曲美替尼——BRAF V600E突變NSCLC一線治療安全、強效的“黃金搭檔”。
BRAF突變與腫瘤不良預後有關,研究證實,BRAF V600突變NSCLC 患者總生存期(OS)明顯短於野生型患者[4,5]。在BRAF V600突變NSCLC患者的治療中,有研究表明化療或免疫治療在客觀緩解率(ORR)和PFS等方面的臨床獲益有限[6,7]。雖然BRAF抑制劑單藥靶向治療BRAF V600突變NSCLC患者展現出抗腫瘤活性,但其治療效果仍不理想[8]。隨著達拉非尼+曲美替尼雙靶方案的獲批,BRAF突變陽性晚期NSCLC的生存瓶頸已被打破。達拉非尼+曲美替尼是針對BRAF和MEK的靶向藥物,聯合用藥能夠從上下遊全面阻斷MAPK通路,從而達到更好的抗腫瘤效果[9,10]。動物實驗也表明,BRAF和MEK抑制劑聯用的協同作用相比各自單藥更加明顯,且部分3/4級不良事件(AE)發生率更低[11]。
BRF113928研究[12,13]是一項國際性、多中心、多隊列、非隨機、開放標簽的II期臨床研究,對比了BRAF抑制劑單藥與BRAF+MEK雙靶組合治療BRAF V600E陽性晚期NSCLC的療效。所有病人接受口服達拉非尼±曲美替尼,21天為一個周期,直至疾病進展。患者被分為三個隊列,隊列A:納入經治的患者,接受達拉非尼單藥治療,共78例;隊列B:納入經治的患者,接受達拉非尼+曲美替尼治療,共57例;隊列C:納入初治的患者,接受達拉非尼+曲美替尼治療,共36例。研究結果顯示,隊列A達拉非尼單藥治療的ORR為33%,而隊列B和隊列C使用達拉非尼+曲美替尼的ORR明顯提高,分別達到了68.4%和63.9%。另外,隊列C初治患者的中位緩解持續時間(DoR)達到了15.2個月,而隊列B經治患者的DoR為9.8個月。在安全性方面,達拉非尼+曲美替尼雙靶治療治療對比單靶治療,任何級別的發熱或胃腸道不良反應雖有所增加,但是3-4級AE發生率和單靶相似,使用達拉非尼+曲美替尼治療中皮膚相關不良反應明顯減少。研究結果提示無論是初治或是經治BRAF患者,雙靶組合都能展現出不錯的療效和安全性。
達拉非尼+曲美替尼一線治療的顯著療效也在真實世界中得到驗證。2022年美國臨床腫瘤學會(ASCO)大會上發佈的一項真實世界研究[14]顯示,一線雙靶治療的ORR為82.9%,中位PFS為18.2個月,中位OS 為24.1個月,優於二線接受雙靶治療的患者。2023年歐洲肺癌大會(ELCC)公佈了達拉非尼聯合曲美替尼用於中國BRAF突變NSCLC患者的真實世界研究數據[15]。結果顯示,達拉非尼+曲美替尼一線治療的中位PFS長達25個月,12個月PFS率為67%,24個月PFS率為52%,超過半數患者服藥超過2年依舊具有臨床獲益。而化療和免疫治療等其他治療方案的中位PFS僅為8~11個月,顯示出靶向治療的壓倒性療效優勢。
基於藥物在中國患者中的療效和安全性數據,2022年3月,達拉非尼聯合曲美替尼方案獲得國傢藥品監督管理局(NMPA)批準,用於治療BRAF V600突變陽性轉移性NSCLC患者,填補了長期以來的治療空白。2023年中國臨床腫瘤學會(CSCO)NSCLC指南將達拉非尼+曲美替尼推薦級別提升至Ⅰ級推薦,成為晚期BRAF V600突變NSCLC患者的一線標準治療方案[3]。
該例為肺腺癌術後轉移患者,在基因檢測明確存在BRAF V600E突變後,接受達拉非尼+曲美替尼一線治療。在治療2個月後,療效達到PR,腫瘤標志物水平顯著下降。患者每2個月定期返院復查,療效持續維持PR,腫瘤標志物水平穩定在較低水平。在治療期間患者出現發熱,屬於常見不良反應,通過及時對癥處理和降低藥量,患者可耐受長期治療,療效不受影響。隨著隨訪時間的進一步延長,該例患者的生存數據將持續更新,期待患者實現高質量長期生存。
點評專傢簡介

卜慶 教授
廣西醫科大學第一附屬醫院
廣西醫科大學第一附屬醫院腫瘤內科 醫學博士 主任醫師
中國南方腫瘤臨床研究協會肺癌專業委員會委員
中國抗癌協會靶向治療專業委員會委員
中國抗癌協會第一屆臨床研究管理學專業委員會委員
廣西臨床腫瘤學會副秘書長
廣西臨床腫瘤學會肺癌專業委員會主任委員
廣西抗癌協會肺癌專業委員會副主任委員
廣西抗癌協會青年委員會副主任委員
廣西醫抗癌協會化療專委會副主任委員
廣西臨床腫瘤學會淋巴瘤專業委員會常務委員
廣西腫瘤生物治療專業委員會常務委員
廣西癌癥康復與姑息治療專業委員會常務委員
廣西醫師協會腫瘤科醫師分會常務委員
廣西醫師協會腫瘤化療醫師分會常務委員
廣西腫瘤性疾病醫療質量控制中心肺癌專傢委員會委員
病例提供專傢簡介

顏雪馨 教授
廣西醫科大學第一附屬醫院
腫瘤內科 主治醫師 醫學碩士
廣西臨床腫瘤學會肺癌專業委員會 委員
廣西臨床腫瘤學會青年委員會 委員
參考文獻
[1] NCCN NSCLC guideline 2022 v6.
[2]Updated version published 15 September 2020 by the ESMO Guidelines Committee.
[3]中國臨床腫瘤學會(CSCO)非小細胞肺癌診療指南2023.
[4] LEONETTI A, FACCHINETTI F, ROSSI G, et al. BRAF in non-small cell lung cancer (NSCLC): pickaxing another brick in the wall[J]. Cancer Treat Rev, 2018, 66: 82-94.
[5] MARCHETTI A, FELICIONI L, MALATESTA S, et al. Clinical features and outcome of patients with non-small cell lung cancer harboring BRAF mutations[J]. J Clin Oncol, 2011, 29(26): 3574-3579.
[6] DUDNIK E, PELED N, NECHUSHTAN H, et al. BRAF mutant lung cancer: programmed death ligand 1 expression, tumor mutational burden, microsatellite instability status, and response to immune check-point inhibitors[J]. J Thorac Oncol, 2018, 13(8): 1128-1137.
[7] DING X, ZHANG Z L, JIANG T, et al. Clinicopathologic characteristics and outcomes of Chinese patients with non-small cell lung cancer and BRAF mutation[J]. Cancer Med, 2017, 6(3): 555-562.
[8] 中國抗癌協會肺癌專業委員會. 中國晚期非小細胞肺癌BRAF突變診療專傢共識[J]. 中華腫瘤雜志, 2023, 45(4):279-290.
[9] Sánchez-Torres JM, Viteri S, Molina MA, Rosell R. BRAF mutant non-small cell lung cancer and treatment with BRAF inhibitors. Transl Lung Cancer Res. 2013;2(3):244-250.
[10] Beeram M, Patnaik A, Rowinsky EK. Raf: a strategic target for therapeutic development against cancer. J Clin Oncol. 2005;23(27):6771-6790.
[11] KING A J, ARNONE M R, BLEAM M R, et al. Dabrafenib; preclinical characterization, increased efficacy when combined with trametinib, while BRAF/MEK tool combination reduced skin lesions[J]. PLoS One, 2013, 8(7): e67583.
[12] Planchard D, Besse B, Groen HJM, et al. Phase 2 Study of Dabrafenib Plus Trametinib in Patients With BRAF V600E-Mutant Metastatic NSCLC: Updated 5-Year Survival Rates and Genomic Analysis. J Thorac Oncol. 2022;17(1):103-115.
[13] Planchard D, Smit EF, Groen HJM, et al. Dabrafenib plus trametinib in patients with previously untreated BRAFV600E-mutant metastatic non-small-cell lung cancer: an open-label, phase 2 trial. Lancet Oncol. 2017;18(10):1307-1316.
[14] Aurelie SWALDUZ et al.2022 ASCO, Poster 9082.
[15] Jia B, Zhao J, Jin B, et al. Prevalence, clinical characteristics, and treatment outcomes of patients with BRAF-mutated advanced NSCLC in China: a real-world multi-center study. 2023 ELCC 36P.
*項目碼:TML0008922;項目失效日:2024-08-26
* 此文僅用於向醫學人士提供科學信息,不代表本平臺觀點